Por Zachary Stieber
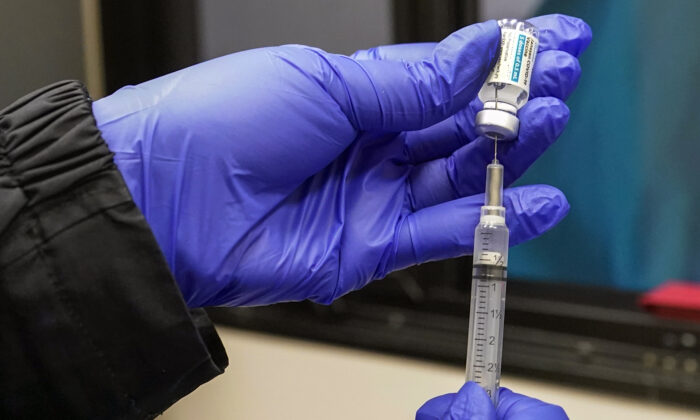
As autoridades de saúde dos EUA estão recomendando que a vacina COVID-19 da Johnson & Johnson não seja usada até que uma investigação sobre os casos de coágulos sanguíneos pós-vacinação seja concluída.
Os seis casos, todos entre mulheres, envolvem um tipo raro e grave de coágulo chamado trombose do seio venoso cerebral em combinação com baixos níveis de plaquetas sanguíneas, de acordo com a Dra. Anne Schuchat, diretora-adjunta principal dos Centros de Controle e Prevenção de Doenças ( CDC )
Os pacientes têm entre 18 e 48 anos. Eles experimentaram coágulos sanguíneos e níveis baixos de plaquetas entre 6 e 13 dias após receber a vacina COVID-19, Schuchat e Dr. Peter Marks, diretor do Food and Drug Administration’s Center for A Avaliação e Pesquisa Biológica disse em um comunicado conjunto na terça-feira.
“No momento, esses eventos adversos parecem ser extremamente raros”, disseram as autoridades de saúde, observando que mais de 6,8 milhões de doses da injeção da Johnson & Johnson foram administradas no país até 12 de abril.
Para responder aos casos, o CDC está convocando uma reunião de seu comitê consultivo de vacinação na quarta-feira para analisá-los e avaliar seu potencial significado. A Food and Drug Administration, junto com a investigação dos próprios casos, revisará essa análise.
“Até que esse processo seja concluído, recomendamos uma pausa no uso desta vacina por muita cautela”, disseram os funcionários.
O tratamento do tipo específico de coágulo sanguíneo é diferente dos tratamentos que podem ser administrados normalmente. Normalmente, os coágulos são tratados com heparina, um medicamento anticoagulante, mas usar o medicamento para tratar a trombose do seio venoso cerebral pode ser perigoso.
Johnson & Johnson disse ao Epoch Times em uma declaração recente que a empresa estava “ciente de que eventos tromboembólicos, incluindo aqueles com trombocitopenia, foram relatados com todas as vacinas COVID-19”, acrescentando: “Nosso rastreamento próximo dos efeitos colaterais revelou um pequeno número de acontecimentos muito raros após a vacinação. No momento, nenhuma relação causal clara foi estabelecida entre esses eventos raros e a vacina Janssen COVID-19. ”
Em uma atualização na terça-feira, a empresa disse que as autoridades de saúde recomendaram uma pausa no uso de sua vacina “por excesso de cautela”. Diante da recomendação, a empresa está atrasando o lançamento de sua vacina na Europa.
“Temos trabalhado em estreita colaboração com especialistas médicos e autoridades de saúde e apoiamos fortemente a comunicação aberta dessas informações aos profissionais de saúde e ao público”, disse Johnson & Johnson.

A vacina da Johnson & Johnson ainda não foi administrada na Europa. Os Estados Unidos foram um dos primeiros países do mundo a autorizar a vacina.
Enquanto as autoridades de saúde estão levantando preocupações sobre coágulos sanguíneos, os reguladores de medicamentos não revogaram a autorização de uso de emergência (EUA), disse o ex-comissário da Food and Drug Administration, Scott Gottlieb, no “Squawk Box” da CNBC.
“Eles não revogaram os EUA, não pediram isso do mercado. Essa foi uma pausa solicitada, o que é uma etapa regulatória incômoda, mas reflete um nível de cautela para não aparecer com muita força aqui ”, disse ele.
A pausa recomendada veio depois que pelo menos quatro locais de vacinação em massa suspenderam a administração de vacinas nos últimos dias por causa de séries de reações adversas após injeções da empresa com sede em Nova Jersey, incluindo Cumming Fairgrounds na Geórgia e PNC Arena na Carolina do Norte.
Outros locais menores também suspenderam as injeções devido a reações semelhantes.
As reações adversas incluíram tonturas, vertigens e sintomas de suor, entre outros, disse um porta-voz do CDC ao Epoch Times por e-mail.
A Agência Europeia de Medicamentos anunciou na semana passada que estava investigando casos de formação de coágulos sanguíneos em pessoas que receberam as vacinas nos Estados Unidos.